La medicina moderna ha avanzado a pasos agigantados, y uno de los pilares fundamentales de este progreso es el proceso de experimentación de nuevos medicamentos. Este proceso no sólo implica la búsqueda de nuevas opciones terapéuticas, sino que también garantiza que los tratamientos disponibles sean seguros y efectivos para los pacientes. A través de metodologías rigurosas, la ciencia médica investiga, prueba y elige tratamientos que pueden cambiar vidas, mejorando la salud y calidad de vida de millones de personas en todo el mundo.
En este artículo, exploraremos en detalle el complejo proceso de experimentación de medicamentos, que va desde la investigación inicial hasta los ensayos clínicos, y finalmente, la aprobación y lanzamiento de nuevos fármacos al mercado. Analizaremos cada etapa del proceso, las regulaciones implicadas, la importancia de la ética en la investigación, y cómo estas prácticas influyen en la innovación médica y la salud pública.
Fases de la Experimentación de Nuevos Medicamentos
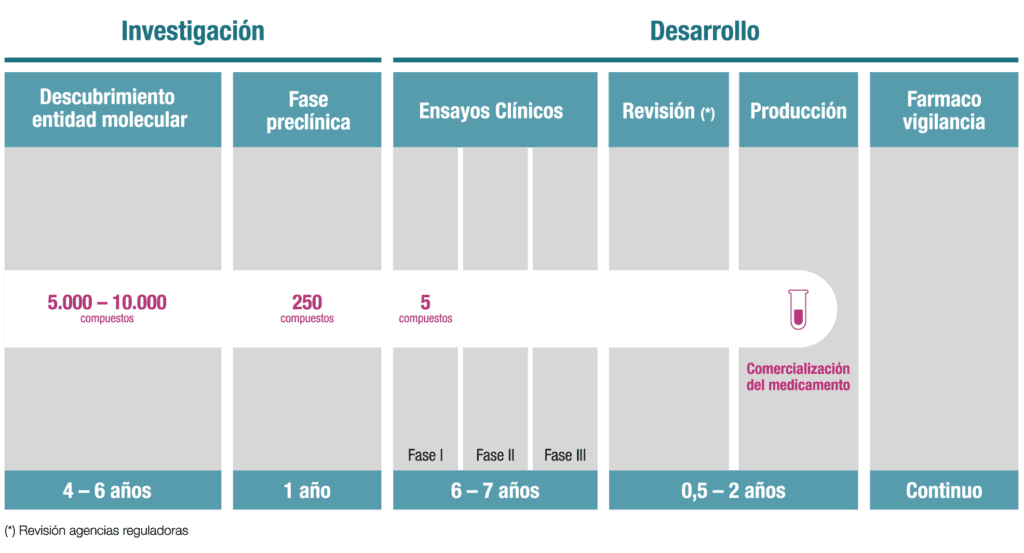
El desarrollo de un nuevo medicamento es un camino largo y complicado, dividido en varias fases clave. La primera fase incluye la investigación básica, donde los científicos buscan entender la biología de una enfermedad y el mecanismo de acción potencial del medicamento. En esta etapa, se emplean modelos celulares y animales para obtener datos sobre la eficacia y toxicidad del compuesto antes de que se considere su uso en humanos.
La siguiente fase, conocida como desarrollo preclínico, establece el fundamento para los ensayos clínicos. En esta etapa, se realizan estudios más sofisticados y se evalúan diferentes dosis del medicamento en modelos animales para evaluar la farmacocinética y farmacodinámica del fármaco. La información recopilada aquí es crucial para determinar la seguridad inicial y establecer un perfil de efectividad que justifique la transición hacia las pruebas en humanos.
Ensayos Clínicos: Una Mirada Profunda
La realización de ensayos clínicos es uno de los pasos más críticos en el proceso de experimentación de medicamentos. Los ensayos clínicos se dividen en varias fases: Fase I, Fase II, Fase III y, en algunos casos, Fase IV. La Fase I está centrada en la evaluación de la seguridad y dosificación del medicamento en un pequeño grupo de voluntarios sanos. Aquí es donde se determina la máxima dosis tolerada y se monitorean los efectos secundarios inmediatos.
En la Fase II, el enfoque cambia hacia un grupo más grande de pacientes que padecen la enfermedad objetivo del medicamento. Esta fase busca establecer la eficacia del fármaco y continuar investigando su seguridad a medida que se obtienen más datos sobre efectos adversos. Los resultados de esta fase son cruciales, ya que si el medicamento no muestra efectividad significativa, es poco probable que continúe hacia la siguiente etapa.
La Fase III es donde se realizan estudios multicéntricos y, a menudo, se involucran miles de pacientes. Este es un período intensivo que proporciona datos robustos sobre la efectividad del medicamento en condiciones del mundo real. Si los resultados son favorables, se recolectan todos los datos necesarios para la presentación ante las autoridades regulatorias, como la FDA en Estados Unidos, para la obtención de aprobación.
Regulaciones y ética en la Experimentación
Las regulaciones que rigen la experimentación con humanos son fundamentales para garantizar la ética y la seguridad en la investigación. Las entidades reguladoras establecen lineamientos que los investigadores deben seguir para preservar la integridad de los ensayos clínicos y la salud de los participantes. Los aspectos éticos son primordiales, lo que incluye obtener el consentimiento informado de todos los participantes y asegurar la confidencialidad de los datos recolectados.
Además, muchas instituciones y compañías farmacéuticas cuentan con comités de ética que revisan todos los protocolos de investigación antes de que se inicien los ensayos, asegurando que todos los criterios necesarios se cumplan para proteger a los voluntarios. El mantenimiento de las normas éticas no solo fortalece la confianza pública en la investigación médica, sino que también promueve la integridad científica y el desarrollo responsable de nuevos tratamientos.
Impacto de la Innovación en la Salud Pública
La experimentación de nuevos medicamentos tiene un impacto profundo en la salud pública, ya que proporciona soluciones efectivas a enfermedades que, de otro modo, podrían ser mortales o incapacitantes. La rápida innovación en farmacología ha llevado al desarrollo de tratamientos para diversas condiciones, desde enfermedades comunes hasta patologías raras. Sin embargo, el proceso no está exento de desafíos.
La notable competencia entre las compañías farmacéuticas a menudo impulsa el desarrollo innovador, pero también puede resultar en prácticas problemáticas, como la manipulación de datos o la priorización de beneficios sobre el bienestar del paciente. A medida que se implementan nuevas tecnologías, como la inteligencia artificial y la biotecnología, se abre un abanico de oportunidades para agilizar el proceso de descubrimiento y mejorar la precisión en las terapias, destacando la necesidad de una regulación robusta y eficaz.
Conclusiones: El Futuro de la Experimentación de Medicamentos
El proceso de experimentación de nuevos medicamentos es una labor compleja que combina avances científicos y tecnológicos, con rigurosas normativas éticas y regulatorias. Desde la investigación básica hasta los ensayos clínicos y la eventual aprobación de nuevos tratamientos, cada fase es esencial para garantizar que los medicamentos sean seguros y eficaces. A medida que continuamos avanzando en este campo, el objetivo debe ser no solo desenvolver innovaciones farmacológicas, sino hacerlo de manera que priorice la salud y el bienestar de los pacientes. El futuro de la medicina dependerá en gran medida de nuestra capacidad para mantener los estándares éticos justo al nivel de nuestra aspiración por la innovación, asegurando que el progreso en medicina beneficie a toda la sociedad.


